肿瘤学国际知名期刊Oncogene(IF=7.9) 2017年4月10日在线报道了我校药学院上海市新药设计重点实验室李剑课题组和黄瑾课题组,在非小细胞肺癌精准治疗研究领域重要成果“Selective targeting p53WT lung cancer cells harboring homozygous p53 Arg72 by an inhibitor of CypA (http://www.nature.com/onc/journal/vaop/ncurrent/full/onc201741a.html)”,此项研究通过大规模药物筛选、肿瘤基因组学分析、细胞信号通路研究和体内药效学评价等方法,发现自主开发的CypA强效小分子抑制剂HL001可以选择性杀伤p53 72R基因型的非小细胞肺癌。Oncogene为肿瘤学四大刊之一,上述论文为我校作为第一单位发表在Oncogene上的第一篇研究论文。
肺癌是全球死亡率最高的恶性肿瘤之一。《2015中国肿瘤统计年报》显示,肺癌也是我国癌症发病率和死亡率最高的肿瘤之一。以EGFR靶向药物等为主的治疗药物在肺癌临床治疗中疗效明确,可有效改善肺癌患者的生存期和生活质量。这些靶向药物的成功为肺癌的精准医疗打下了坚实的基础,然而以上药物仅对少部分的EGFR突变活化的肺癌病人有效。因此,我们亟需寻找作用于肺癌发生发展关键靶蛋白的新型靶向药物,为更多的肺癌病人实现精准医疗。
癌症基因组学和临床病理学的研究结果明确显示 CypA表达量和肿瘤发生发展具有显著的相关性,CypA在肺癌中存在过量表达,并且对正常细胞的转化、肿瘤的发展和转移起促进作用。同时,CypA的过量表达可使肺癌细胞对化疗药物产生耐药性。因此,CypA是具有良好开发前景的新型肺癌精准治疗药物靶点,开发特异性的CypA抑制剂有望应用于肺癌的临床治疗。
在上海药物研究所蒋华良研究员等指导下,2006年李剑报道了系列非肽类小分子CypA抑制剂(Bioorg Med Chem. 2006, 14, 2209-2224、J Comb Chem. 2006, 8, 326-337、Bioorg Med Chem. 2006, 14, 5527-5534)。基于这些前期研究结果,李剑、黄瑾与北京大学裴剑锋等合作,在科技部863计划(2006AA020404)资助下,应用自主研发的化合物从头设计软件LigBuilder,成功发现了全新结构、具有纳摩尔活性的小分子CypA抑制剂,也是目前国际上报道的活性最强的非肽类小分子CypA抑制剂(J Med Chem. 2009, 52, 5295-5298)。
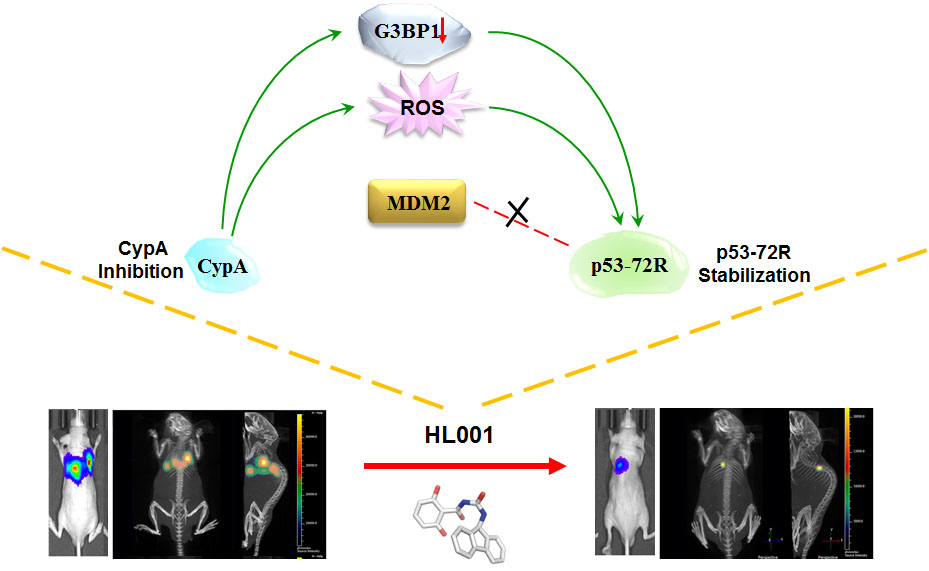
在国家自然科学基金委重大研究计划“基于化学小分子探针的信号转导过程研究”培育项目(90813005)和集成项目(91313303)的进一步资助下,李剑与黄瑾深入合作发现,CypA可通过与G3BP1的相互作用,调节肺癌细胞中抑癌基因p53的功能。CypA 抑制剂HL001可通过诱导野生型p53的表达,显著抑制肺癌细胞的增殖,并首次发现HL001可通过调控CypA/p53 72R/MDM2信号通路,在体内外选择性杀伤p53 72R型肺癌细胞。HL001与化疗药物顺铂联用,在小鼠原位瘤模型中,可以协同强效抑制肺癌A549原位移植瘤的生长。杀伤特定基因型的肿瘤是目前抗肿瘤药物的研发趋势,CypA 抑制剂选择性杀伤肺癌细胞的特性将赋予该类化合物良好的开发潜能,HL001有望成为肺癌精准医疗研究的药物候选物或工具分子(李剑,黄瑾等. CN105326821A)。
上述研究论文的第一作者为黄瑾课题组的卢伟强博士(现华东师范大学)、李剑课题组的闫文仲博士(现上海科技大学博士后)及美国哈佛医学院程飞雄博士(博士毕业于药学院唐赟课题组)。本论文的完成得到了华东理工大学药学院唐赟教授的大力帮助和支持。